Persaingan di Mash memanas saat GLP-1S GATE-BRASH pesta
Komposit digital dari hati wanita yang menyakitkan merah yang disorot | Kredit gambar: © mi_viri -stock.adobe.com
Steatohepatitis terkait disfungsi metabolik (tumbuhan) adalah jenis penyakit hati berlemak non-alkohol (NAFLD) yang mempengaruhi lebih dari 250 juta orang di seluruh dunia, dan jumlah kasus dalam tahap lanjut diperkirakan akan berlipat ganda pada tahun 2030. Kondisi yang mendasarinya seperti obesitas, diabetes tipe 3, dan syndrome metabolik dapat meningkatkan risiko ini. Selama bertahun-tahun, tumbuk sulit diobati, dan beberapa produk telah gagal dalam pengembangan klinis, termasuk agonis proliferator-teraktivasi peroxisome (PPAR) agonis elafibranor, inhibitor con-con-con-con-con-con-con-con-con-con-con-con-con-con-con-con-con-con-con.
Apa saja persetujuan produk terbaru?
Dalam beberapa tahun terakhir, kemajuan yang signifikan telah dibuat, dan produk -produk baru telah memasuki pasar mash. Pada bulan Maret 2024, Administrasi Makanan dan Obat AS (FDA) menyetujui Madrigal Pharmaceuticals yang aktif secara oral, reseptor hormon tiroid selektif (THR) -β agonis, rezdiffra (resmetirom), untuk orang dewasa dengan tumbuk dengan scaring hati sedang hingga lanjut (fibrosis), di samping diet dan latihan (1). Pada bulan Juni 2025, Komite Obat -obatan Eropa (EMA) untuk Produk Obat untuk Penggunaan Manusia (CHMP) merekomendasikan pemberian otorisasi pemasaran bersyarat untuk Rezdiffra di Mash (2). Pada 19 Agustus 2026, Komisi Eropa menyetujui Rezidiffra, dan perusahaan sedang merencanakan peluncuran Eropa pertamanya di Jerman pada kuartal keempat 2025 (4).
Pada bulan Agustus 2025, Novo Nordisk menerima persetujuan FDA untuk obat penurunan berat badan yang dapat disuntikkan (semaglutide) untuk pasien dengan mash dan fibrosis hati yang sedang hingga lanjut, tanpa sirosis, dalam kombinasi dengan diet dan olahraga yang berkurang (4). Clearance conditional didasarkan pada hasil fase III, di mana agonis reseptor peptida-1 seperti glukagon (GLP-1RA) menunjukkan peningkatan jaringan parut hati tanpa memperburuk kondisi dan terselesaikan tumbuk tanpa membuat jaringan parut lebih buruk (5,6). Eli Lilly juga mencari persetujuan untuk suntik ganda-aksi lambung polipeptida (GIP)/GLP-1RA, Zepbound (Tirzepatide), berdasarkan uji coba sinergis fase II pada pasien dengan dan tanpa diabetes tipe 2, dan dengan stadium 2 atau 3 fibrosis (kecari) (7.8).
Investasi apa yang dilakukan farmasi besar di tumbuk?
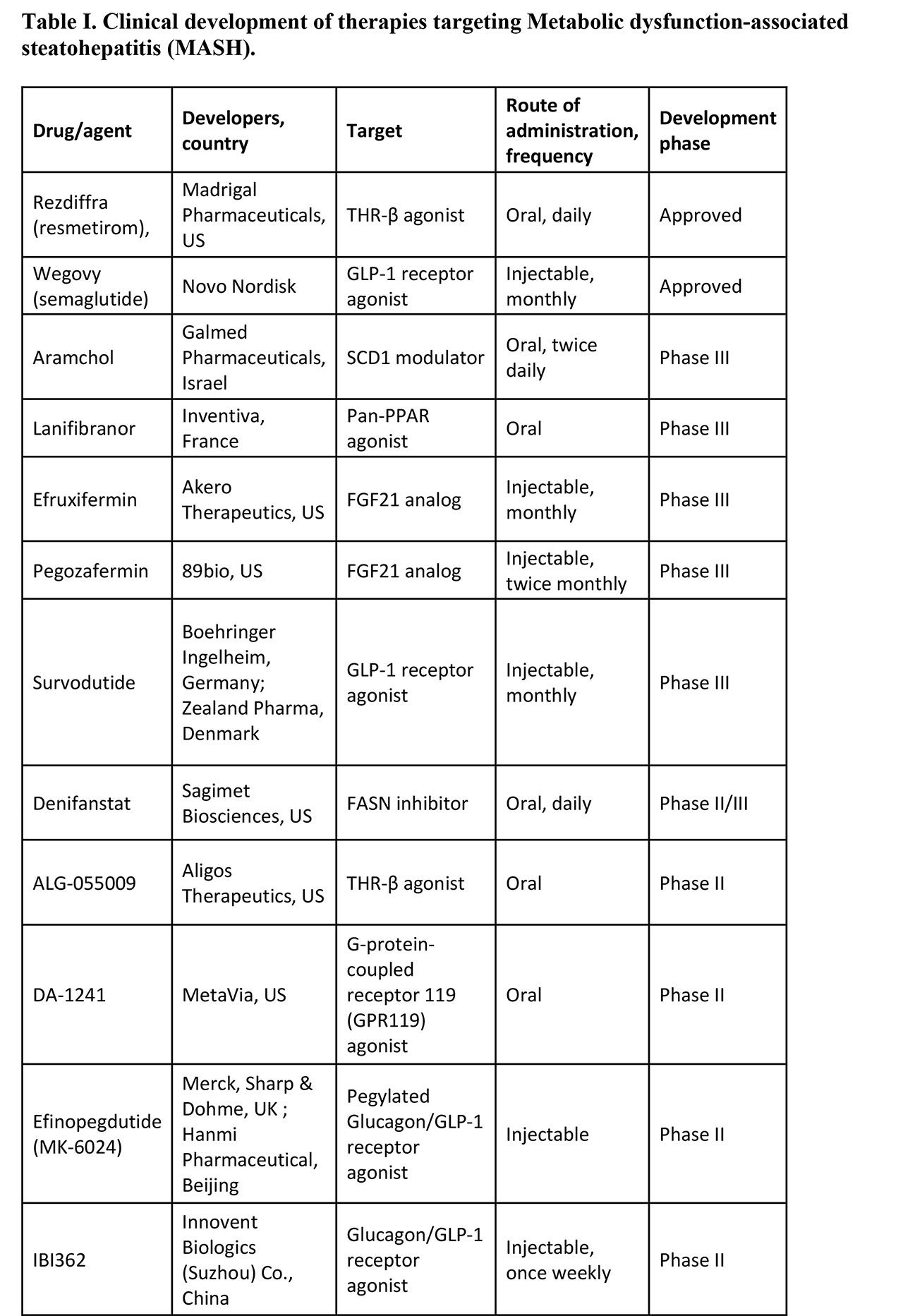
Tumbuk dipandang sebagai perbatasan berikutnya dalam penyakit metabolik, dan banyak uji klinis sedang berlangsung mengevaluasi analog hormon, agonis reseptor, dan inhibitor enzim (Tabel I). Pengembangan obat mash telah menarik minat yang signifikan dari investor farmasi dan swasta. Di ruang GLP-1, Boehringer Ingelheim telah bekerja sama dengan Selandia Pharma yang berbasis di Inggris untuk mengembangkan Survodutide. Agonis Glucagon/GLP-1 ganda ini telah menunjukkan peningkatan 64,8% yang disesuaikan dengan plasebo pada penyakit hati berlemak (9).
Tabel I. Perkembangan klinis terapi yang menargetkan steatohepatitis terkait disfungsi metabolik.
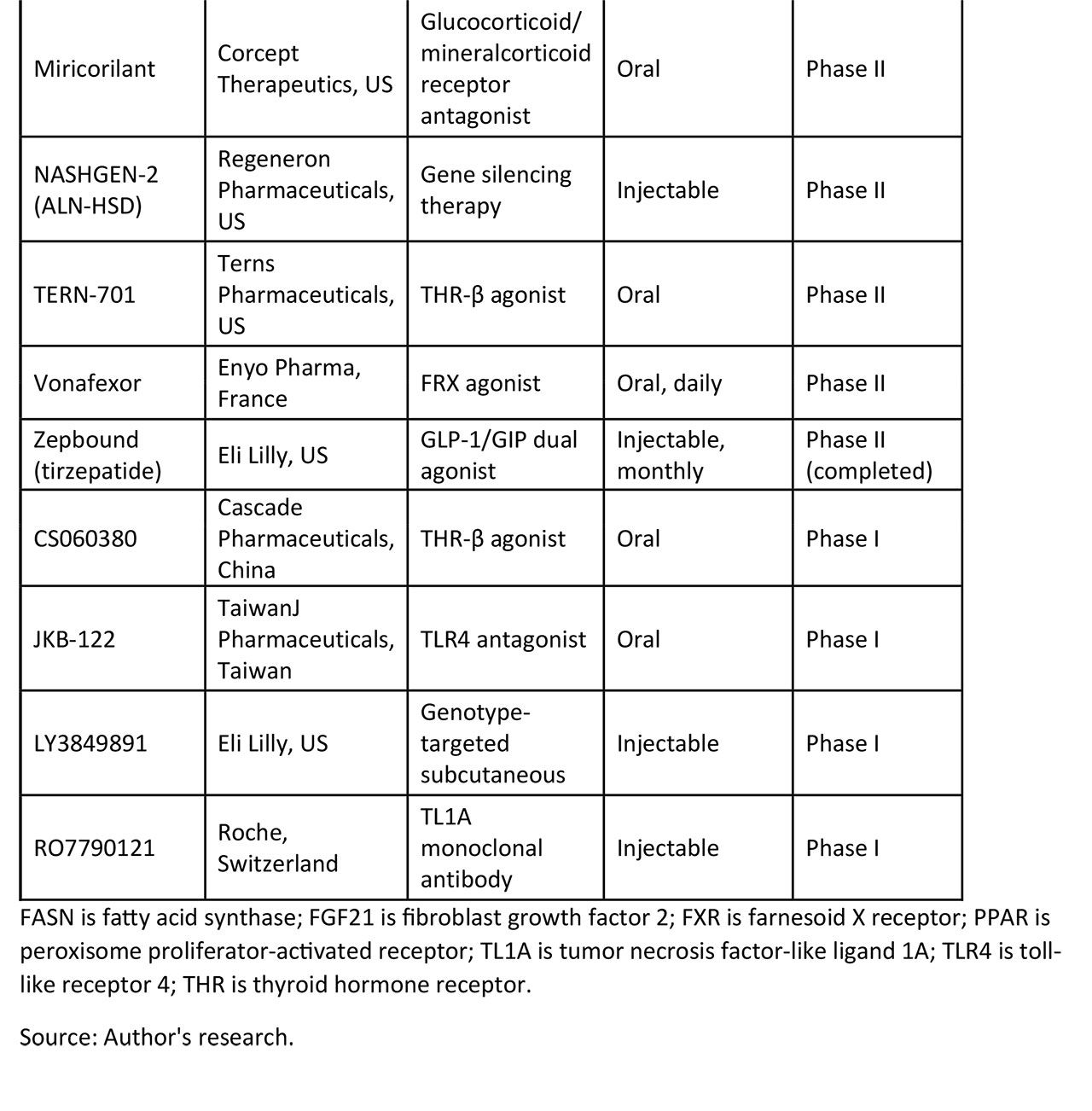
Tabel I. Perkembangan klinis terapi yang menargetkan steatohepatitis terkait disfungsi metabolik (MASH) (lanjutan).
Pada Mei 2025, GSK mengakuisisi Efimosfermin aset utama Boston Pharmaceuticals untuk US $ 1,2 miliar ditambah US $ 800 juta dalam pembayaran tonggak. Efimosfermin adalah terapi analog fibroblast yang baru, sekali bulanan (FGF21) analog dalam pengembangan klinis fase II untuk pengobatan tumbuk (10). Terapeutik Akero yang berbasis di AS dan 89bio juga mengembangkan analog FGF21, eFruxifermin dan pegozafermin, masing-masing (11, 12).
Pelopor Eropa mana yang menargetkan tumbuk?
Beberapa biotek Eropa sedang mengembangkan pendekatan inovatif untuk menargetkan penyebab mendasar dari mash dan fibrosis hati. Ini termasuk:
- Penemuan, Prancis, Berfokus pada pengembangan terapi molekul kecil baru yang menargetkan fibrosis, gangguan penyimpanan lisosom, dan onkologi. Program utama, Lanifibranor (IVA337), adalah agonis pan-PPAR yang aktif secara oral. Ini menunjukkan hasil yang menjanjikan dalam percobaan yang dikendalikan plasebo fase IIB pada pasien dengan tumbuk aktif, meningkatkan resolusi tumbuk tanpa memburuknya fibrosis (13). Lanifibranor saat ini sedang dievaluasi dalam Nativ3, uji klinis fase III yang penting pada pasien dengan tahap tumbuk dan fibrosis F2 dan F3; Percobaan akan selesai pada bulan September 2026 (14).
- Enyo Pharma, Prancis, adalah perusahaan biofarmasi tahap klinis yang berspesialisasi dalam penyakit fibrolitik dan anti-inflamasi. Senyawa timbalnya, vonafexor, adalah agonis non-steroid yang aktif secara oral dari NR1H4 (FXR, atau reseptor asam empedu). Dalam studi fase II penghancuran, vonafexor secara signifikan mengurangi fibrosis hati dan penanda peradangan, penurunan lemak dan berat hati, dan peningkatan fungsi hati dan ginjal (15). Pada Januari 2024, perusahaan mengumpulkan € 39 juta (US $ 45,39 juta) dalam pendanaan Seri C untuk mengembangkan Vonafexor lebih lanjut (16).
- Selandia Pharma, Denmarkadalah perusahaan bioteknologi yang berfokus pada menemukan dan mengembangkan obat-obatan berbasis peptida inovatif. Ini telah menciptakan beberapa kandidat yang menargetkan sumbu otak metabolik, termasuk Survodutide, agonis ganda Glucagon/GLP-1, yang sedang dikembangkan dengan Boehringer Ingelheim untuk tumbuk (fase II) dan obesitas (fase II), dan petrelintide, analog amilin yang dikembangkan bersama dengan roche. Senyawa ini dapat mewakili kelas pengobatan baru untuk obesitas (17).
Di Amerika Serikat, beberapa perusahaan biotek sedang mengerjakan kandidat tumbuk, termasuk Metavia, yang mengembangkan DA-1726, analog oxyntomodulin (OXM) baru yang berfungsi sebagai reseptor peptida-1 seperti glukagon (GLP1R) dan agonis ganda (18).
Diagnostik tumbuk online
Selain itu, kemajuan yang signifikan telah dibuat dalam mengembangkan biomarker dan diagnostik untuk mengidentifikasi pasien yang berisiko tumbuk. Misalnya, GenFit yang berbasis di Perancis telah menciptakan program diagnostik non-invasif yang mencakup in vitro Tes untuk mendeteksi NIS4+ dan NIS2+. Pada saat yang sama, Nordic Bioscience telah mengidentifikasi biomarker yang menargetkan neo-epitop fragmen kolagen yang dapat digunakan untuk stratifikasi risiko pasien. (19, 20).
Masa depan tumbuk
Pasar mash global bernilai US $ 7,9 miliar pada tahun 2024 dan diperkirakan akan tumbuh menjadi US $ 31,8 miliar pada tahun 2033, dengan tingkat pertumbuhan tahunan majemuk 17,7% dari tahun 2025 hingga 2033 (21). Setelah banyak upaya yang gagal, industri akhirnya mengidentifikasi cara -cara baru untuk mengurangi penumpukan lemak hati. Sementara Rezdiffra Madrigal yang aktif secara lisan adalah orang pertama yang memasuki pasar AS dan Uni Eropa, sekarang menghadapi persaingan dari Wegovy yang disuntikkan Novo, dan Eli Lilly tidak jauh di belakang. Akan menarik untuk melihat bagaimana lanskap mash berkembang dan apakah pendekatan baru, seperti analog oxyntomodulin dan agen pembungkaman gen, dapat menangkap pangsa pasar yang menguntungkan ini di masa depan.
Referensi
- FDA. FDA menyetujui pengobatan pertama untuk pasien dengan jaringan parut hati karena penyakit hati berlemak. Siaran pers. 14 Maret 2024.
- Ema. Rezdiffra. Ema.europa.eu. 20 Juni 2025
- Farmasi Madrigal. Madrigal menerima persetujuan Komisi Eropa untuk Rezdiffra ™ (Resmetirom) untuk pengobatan tumbuk dengan fibrosis hati sedang hingga lanjut. Siaran pers. 19 Agustus 2025.
- Farmasi Madrigal. Madrigal Pharmaceuticals melaporkan hasil keuangan 2025 kuartal kedua dan memberikan pembaruan perusahaan. Siaran pers. 5 Agustus 2025.
- FDA. FDA menyetujui pengobatan untuk penyakit hati serius yang dikenal sebagai 'mash'. Siaran pers. 15 Agustus 2025
- Sanyal, AJ; Newsome, PN; Kliers, i.; et al. Percobaan fase 3 semaglutide dalam steatohepatitis terkait disfungsi metabolik. The New England Journal of Medicine, 2025 392(21), 2089–2099.
- Novo Nordisk. Semaglutide 2,4 mg menunjukkan peningkatan superior pada fibrosis hati dan resolusi tumbuk dalam uji coba esensi. Siaran pers. 1 November 2024.
- Loomba, R.; Hartman, ML; Lawitz, EJ; et al. (2024). Tirzepatide untuk steatohepatitis terkait disfungsi metabolik dengan fibrosis hati. The New England Journal of Medicine, 2024 391(4), 299–310.
- Boehringer Ingelheim. Survodutide US FDA Breakthrough Therapy Tahap 3 Uji Coba. Siaran pers. 8 Oktober 2024.
- GSK. GSK untuk memperoleh efimosfermin, obat khusus terbaik di kelas terbaik untuk mengobati dan mencegah perkembangan penyakit hati steatotic (SLD). Siaran pers. 14 Mei 2025.
- Terapi Akero. Efruxifermin untuk tumbuk. akerotx.com/clinical-rials (diakses 20 Agustus 2025).
- 89bio. 89Bio menerima status EMA Prime untuk Pegozafermin dalam pengobatan steatohepatitis terkait disfungsi metabolik (tumbuk) dengan fibrosis dan sirosis kompensasi. Siaran pers. 27 Maret 2024.
- Francque, SM; Bedossa, P.; Ratziu, V.; et al .. Sebuah uji coba acak dan terkontrol dari agonis Pan-PPAR Lanifibranor di Nash. The New England Journal of Medicine, 2021 385(17), 1547–1558.
- Clinicaltrials.gov. Detail Studi | Sebuah studi fase 3 yang mengevaluasi kemanjuran dan keamanan lanifibranor diikuti oleh ekstensi pengobatan aktif pada pasien dewasa dengan (NASH) dan fibrosis tahap F2 dan F3 (Nativ3) (diakses 21 Agustus 2025).
- Ratziu, V.; Harrison, SA; Loustaud-Ratti; et al. Perbaikan hepatik dan ginjal dengan agonis FXR vonafexor pada individu dengan dugaan fibrotik nash. Jurnal Hepatologi, 2023 78(3), 479–492.
- Enyo Pharma. Enyo Pharma mengumumkan pembiayaan € 39 juta Seri C dan izin FDA untuk memajukan Vonafexor dalam uji klinis fase 2 untuk pasien dengan sindrom Alport. Siaran pers. 3 Januari 2024.
- Farmasi Selandia. H1 2025 Presentasi. Zealandpharma.com. 14 Agustus 2025.
- Metavia. Dosis Metavia Pasien Pertama dalam kohort MAD 48 mg dari uji klinis fase 1 yang mengevaluasi DA-1726 untuk pengobatan obesitas untuk lebih mengeksplorasi dosis maksimum yang ditoleransi. Siaran pers. 9 Juli 2025
- Genfit. Diagnostik. Genfit.com (diakses 21 Agustus 2025).
- Nordic Bioscience. Masld, Sld, dan tumbuk. nordicbioscience.com (diakses 21 Agustus 2025).
- Kecerdasan Data. Tingkat pertumbuhan pasar Nash atau Mash Treatment, wawasan industri dan perkiraan 2025-2033. April 2025.
Tentang penulis
Cheryl Barton, PhD, adalah pendiri dan Direktur Pharmavision, Pharmavision.co.uk.